在骨科和牙科领域,大块骨缺损的修复一直是一个严峻的挑战。无论是严重的创伤、肿瘤切除,还是先天性疾病,当骨骼的“空洞”大到无法自行愈合时,就需要借助人工支架来引导新骨生长。然而,一个长期被忽视的“隐形杀手”常常在植入早期就扼杀了再生的希望——缺氧。
想象一下,当你将一颗充满生命力的种子(细胞)植入一片贫瘠的土壤(骨缺损区),却发现这片土壤严重缺乏空气(氧气)。种子不仅无法生长,甚至会迅速死亡。在骨缺损区域,尤其是在血管尚未长入的早期阶段,情况正是如此。缺氧环境会直接导致植入的细胞或招募来的细胞死亡,抑制其分化为成骨细胞的能力,并阻碍后续的血管生成,最终导致骨再生失败。
传统的骨修复材料,如金属、陶瓷或聚合物支架,主要关注机械支撑和生物相容性,却很少能主动应对这一早期缺氧危机。近年来,科学家们尝试将能释放氧气的物质(如过氧化钙)掺入材料中,但新的问题随之而来:氧气释放往往“一泻千里”,在初期形成具有毒性的高氧和氧化应激环境,随后又迅速耗尽,无法持续护航整个修复过程。
那么,能否设计一种“智能”支架,既能像呼吸一样平缓、持续地释放氧气,缓解早期缺氧,又能为细胞生长提供一个理想的三维家园?近期,得克萨斯大学奥斯汀分校Maryam Tilton教授带领团队在《Advanced Healthcare Materials》发表的名为《Visible Light Induced DLP-Printed Oxygen-Releasing TPMS Scaffolds Mitigate Early Hypoxia in Bone Defects》研究给出了令人振奋的答案。研究团队成功开发了一种名为 COSnPPOD 的新型复合支架,它巧妙地将可控释氧纳米技术、仿生几何结构与先进3D打印工艺融为一体,为骨再生带来了新的曙光。
三大创新:构筑智能骨再生微环境
这项研究的核心在于三个层面的协同创新,共同构建了一个支持骨再生的理想微环境。
1. 纳米级的“微型氧气工厂”:可控释氧系统
研究的关键在于如何安全、可控地输送氧气。团队没有简单地将释氧物质混合到材料中,而是设计了一个精巧的纳米级输送系统。
他们选择了过氧化钙作为氧气源。当CaO₂遇水时,会缓慢反应生成氧气和氢氧化钙。但直接使用CaO₂粉末,反应难以控制。为此,研究人员扮演了“纳米工程师”的角色,将CaO₂晶体封装进中空的二氧化硅纳米颗粒中。
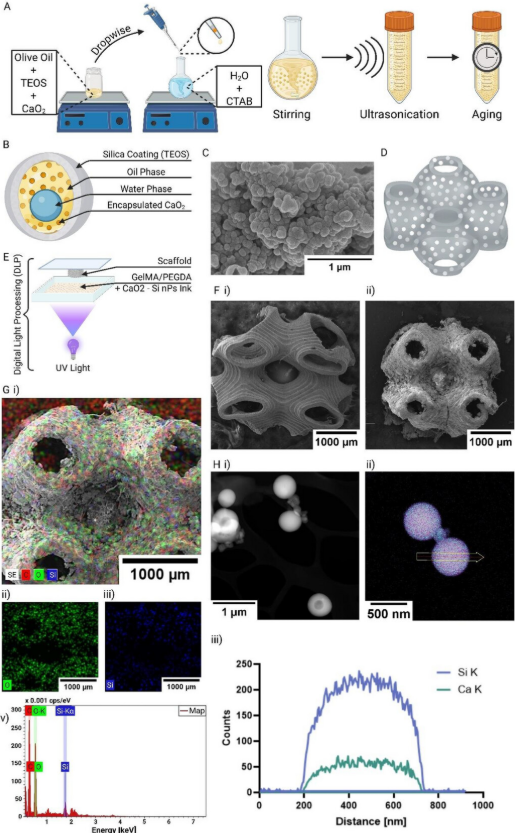
CaO₂-SiO₂纳米颗粒合成及COSnPPOD支架制造流程示意图。左:CaO₂被封装进中空二氧化硅壳中,形成核壳结构纳米颗粒。右:负载纳米颗粒的GelMA-PEGDA生物墨水通过DLP 3D打印成TPMS支架。
这个二氧化硅外壳起到了“智能阀门”的作用。它允许水分子缓慢渗入,与内部的CaO₂反应,同时控制反应产物(氧气和副产物过氧化氢)的释放速率。这样一来,就避免了氧气的爆发式释放,实现了持续、温和的供氧。副产物氢氧化钙还能轻微碱化局部环境,可能对成骨有益;而过氧化氢的释放也受到调控,将其浓度控制在可促进细胞信号传导而非造成毒性的范围内。
2. 模仿自然的“生命骨架”:TPMS仿生结构
如果只有氧气,细胞就像拥有充足空气却无处落脚的浮萍。因此,支架的物理结构至关重要。研究团队放弃了传统的简单孔道结构,转向了自然界的灵感——三周期极小曲面。
TPMS是一种在自然界中广泛存在的复杂而优美的结构,例如蝴蝶翅膀的鳞片、海胆的骨骼。本研究采用的 Primitive型TPMS,其特点在于具有连续、光滑、无死角的曲面,以及高度互连的多孔网络。
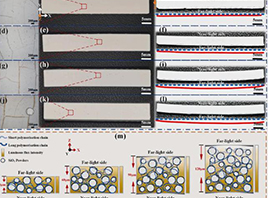
TPMS支架的微观结构(SEM图像)。左:支架整体的三维多孔结构,显示高度有序和互连的孔道。右:更高倍率下支架表面的微观形貌,可见其光滑的曲面特征。
这种结构有何优势?
* 最大化物质交换: 高度互连的孔道确保了营养物质和氧气能够均匀扩散到支架的每一个角落,代谢废物也能被及时运走,完美模拟了天然骨组织中的血管网络功能。
* 促进细胞行为: 连续的曲面更利于细胞粘附、铺展和迁移。细胞可以沿着曲面自由爬行,均匀地占据整个支架,而不是仅仅聚集在表面或棱角处。
* 化机械性能: TPMS结构可以在保证高孔隙率(利于细胞长入)的同时,提供优异的力学性能,其结构刚度可以通过调整参数进行设计,以匹配目标骨组织的力学需求。
3. DLP 3D打印:从设计到实体
将上述精妙的纳米设计和复杂的几何结构变为现实,需要强大的制造工具。研究人员采用了数字光处理 3D打印技术,并使用可见光作为固化光源。
他们制备了一种特殊的“生物墨水”,主要成分是明胶甲基丙烯酰胺和聚乙二醇二丙烯酸酯。GelMA提供良好的细胞相容性和生物活性位点,PEGDA则增强墨水的可打印性和机械强度。最关键的是,将前述合成的CaO₂-SiO₂纳米颗粒均匀分散在这种墨水中。
在打印时,可见光投影仪将TPMS结构的切片图案投射到液态生物墨水槽中,被照射区域的墨水发生光交联固化,平台逐层上升,最终“雕刻”出结构精确、负载着纳米氧气工厂的复杂三维支架。可见光相比紫外光,对细胞和生物分子的损伤更小,为将来直接打印包含活细胞的支架奠定了基础。
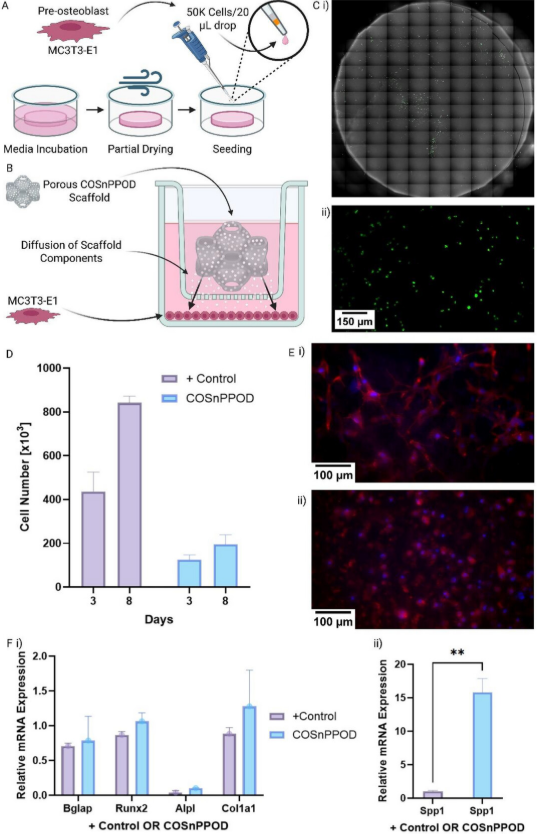
细胞在COSnPPOD支架上的生长情况。左:活死细胞染色显示大部分细胞存活(绿色),证明材料无毒性。右:细胞骨架染色显示细胞在TPMS结构的曲面上良好铺展和迁移。
实验验证:从体外性能到体内疗效
理论设计是否成功,需要严格的实验来检验。
体外测试表明,COSnPPOD支架具有良好的降解性,其刚度可调,并能吸附更多的蛋白质(这有利于细胞粘附)。最重要的是,释氧测试证实了其可控、持续的氧气释放能力,而非短暂的爆发。
在细胞实验中,成骨前体细胞在COSnPPOD支架上活力旺盛,显示出良好的粘附和铺展。尽管常规的成骨基因表达标志物变化不显著,但一个关键基因——骨桥蛋白的表达量惊人地上调了16倍。骨桥蛋白是细胞外基质重塑和矿化初期的重要蛋白,这一结果强烈暗示,COSnPPOD支架提供的微环境(可能是氧气、钙离子、结构的协同作用)特别擅长激活细胞启动组织重建程序。
最有力的证据来自动物实验。研究人员在小鼠颅骨上制造了一个临界尺寸的骨缺损(无法自行愈合),然后植入COSnPPOD支架。
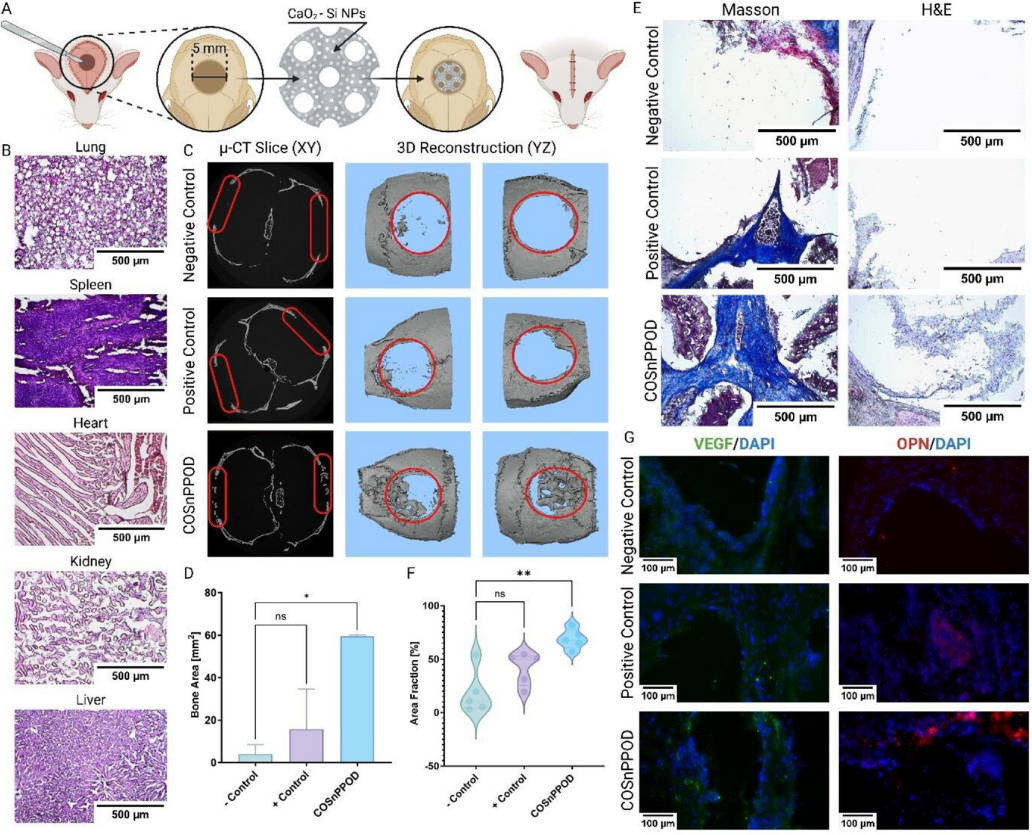
小鼠颅骨缺损模型体内实验结果。上排:Micro-CT三维重建显示,植入COSnPPOD支架(右)的缺损区域新生骨量(白色)远多于空白对照组(左)和单纯水凝胶组(中)。下排:组织切片染色(如Masson三色染)显示COSnPPOD组有更丰富的胶原沉积(蓝色)和骨组织形成。
8周后的结果令人振奋:
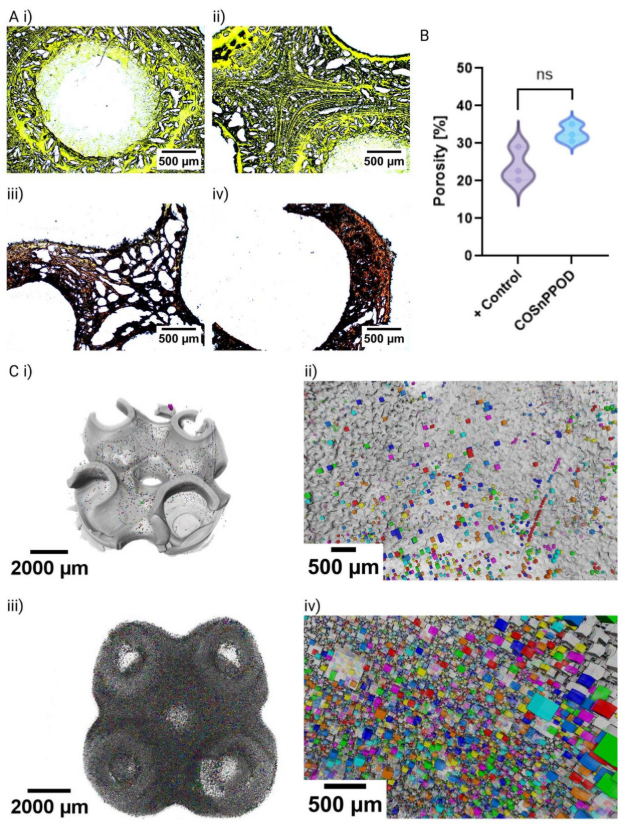
* 骨再生显著增强: Micro-CT扫描和三维重建定量分析显示,COSnPPOD组的新骨生成量显著高于未处理组和仅植入普通水凝胶支架的对照组。组织切片也观察到更密集的胶原沉积和更成熟的骨基质。
* 血管生成反应活跃: 对缺损区域组织的分析发现,血管内皮生长因子(VEGF,促血管生成的关键信号蛋白)的表达明显增强。这表明,缓解早期缺氧不仅直接帮助了成骨细胞,还激活了机体自身的血管生成程序,为后续的骨组织成熟和功能化铺平了道路。
* 安全性良好: 在整个实验期间,未观察到与植入物相关的全身毒性或强烈炎症反应。
结论与展望:迈向下一代骨修复材料
这项研究成功地证明,通过材料学、纳米技术、仿生学和先进制造的交叉融合,可以创造出能够主动干预并优化再生微环境的智能生物材料。COSnPPOD支架系统不仅是一个被动的“填充物”,更是一个能感知并响应早期缺氧危机的主动式治疗平台。
它为解决大段骨缺损修复中的早期血管化难题提供了一个全新的思路:既然等待血管长入太慢,何不先为细胞送去“便携式氧气瓶”,为血管生长赢得时间和创造有利条件?
当然,这项技术走向临床还有一段路要走。未来的研究需要进一步优化氧气释放的动力学,例如,能否实现与细胞耗氧速率相匹配的按需释放?释氧的最佳持续时间和总剂量是多少?此外,在更大、负重部位(如股骨、胫骨)的骨缺损模型中进行测试,以及探索与干细胞、生长因子等其他治疗手段的联合应用,都是值得探索的方向。
无论如何,这项研究标志着骨组织工程领域的一个重要进步:从构建静态的“细胞房子”,到设计动态的、支持生命的“细胞生态系统”。随着这类智能材料的不断发展,未来医生或许能够像打印一个定制零件一样,为患者打印出自带“生命支持系统”的骨骼,让严重骨缺损的完美修复不再是梦想。